Номер 180, страница 212 - гдз по химии 10-11 класс задачник Еремин, Дроздов

Авторы: Еремин В. В., Дроздов А. А., Ромашов Л. В.
Тип: Задачник
Издательство: Просвещение
Год издания: 2023 - 2025
Цвет обложки: белый, зелёный
ISBN: 978-5-09-109700-9
Популярные ГДЗ в 10 классе
Тема 7. Элементы-неметаллы и их соединения. 7.3. Элементы V группы. 7.3.1. Азот. Уровень 1 - номер 180, страница 212.
№180 (с. 212)
Условие. №180 (с. 212)
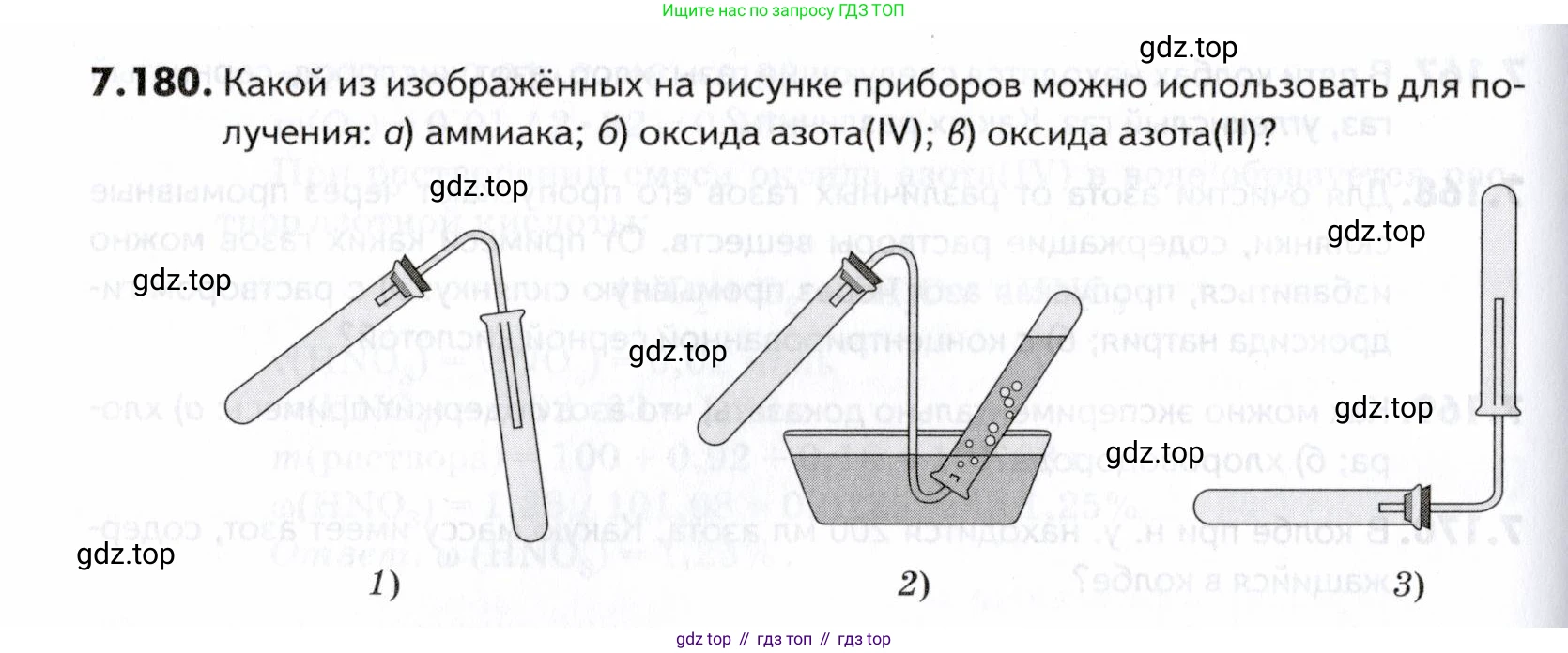
7.180. Какой из изображённых на рисунке приборов можно использовать для получения: а) аммиака; б) оксида азота(IV); в) оксида азота(II)?
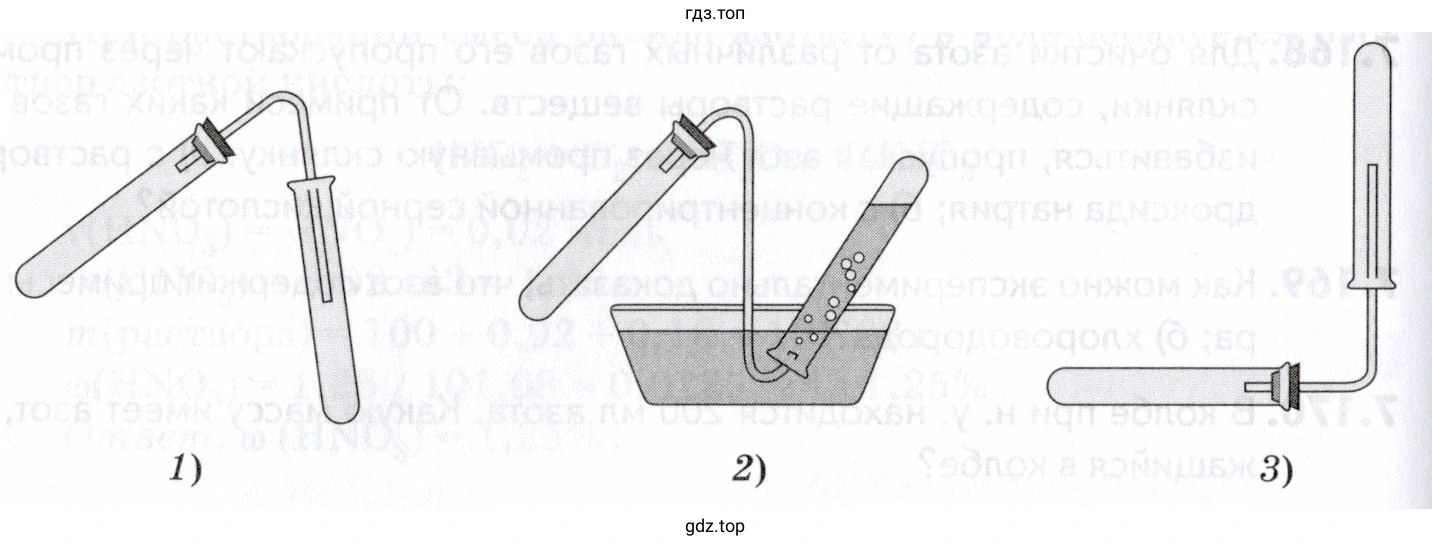
Решение 3. №180 (с. 212)
Чтобы определить, какой прибор подходит для получения каждого из указанных газов, необходимо рассмотреть их ключевые физико-химические свойства: плотность относительно воздуха и растворимость в воде (а также химическую активность).
Средняя молярная масса воздуха принимается равной $M_{возд} \approx 29$ г/моль. Газы с меньшей молярной массой легче воздуха, а с большей — тяжелее.
Анализ приборов:
- Прибор 1: Собирание газа в перевёрнутую пробирку методом вытеснения воздуха. Этот способ (вытеснение воздуха вниз) подходит для газов, которые легче воздуха.
- Прибор 2: Собирание газа методом вытеснения воды. Этот способ подходит для газов, которые нерастворимы или малорастворимы в воде и не реагируют с ней.
- Прибор 3: Собирание газа в пробирку, расположенную отверстием вверх, методом вытеснения воздуха. Этот способ (вытеснение воздуха вверх) подходит для газов, которые тяжелее воздуха.
а) аммиака
Аммиак имеет формулу $NH_3$.
Его молярная масса: $M(NH_3) = 14 + 3 \cdot 1 = 17$ г/моль.
Так как $M(NH_3) = 17$ г/моль, что меньше молярной массы воздуха ($17 < 29$), аммиак значительно легче воздуха.
Аммиак также чрезвычайно хорошо растворим в воде, поэтому его нельзя собирать методом вытеснения воды (прибор 2).
Поскольку аммиак легче воздуха, для его сбора подходит метод вытеснения воздуха вниз, который реализован в приборе 1.
Ответ: для получения аммиака можно использовать прибор, изображённый на рисунке 1.
б) оксида азота(IV)
Оксид азота(IV), или диоксид азота, имеет формулу $NO_2$.
Его молярная масса: $M(NO_2) = 14 + 2 \cdot 16 = 46$ г/моль.
Так как $M(NO_2) = 46$ г/моль, что больше молярной массы воздуха ($46 > 29$), диоксид азота тяжелее воздуха.
Он также реагирует с водой с образованием азотной и азотистой кислот: $2NO_2 + H_2O \rightarrow HNO_3 + HNO_2$. Поэтому его нельзя собирать над водой (прибор 2).
Поскольку $NO_2$ тяжелее воздуха, для его сбора подходит метод вытеснения воздуха вверх, который реализован в приборе 3.
Ответ: для получения оксида азота(IV) можно использовать прибор, изображённый на рисунке 3.
в) оксида азота(II)
Оксид азота(II), или монооксид азота, имеет формулу $NO$.
Его молярная масса: $M(NO) = 14 + 16 = 30$ г/моль.
Его молярная масса очень близка к молярной массе воздуха ($30 \approx 29$), что делает сбор вытеснением воздуха неэффективным.
Самое важное свойство $NO$ — его способность легко окисляться кислородом воздуха до бурого газа $NO_2$: $2NO + O_2 \rightarrow 2NO_2$. Это исключает возможность его сбора в контакте с воздухом (приборы 1 и 3).
При этом оксид азота(II) плохо растворим в воде.
Следовательно, единственно верным способом его сбора из представленных является метод вытеснения воды (прибор 2), который изолирует газ от воздуха.
Ответ: для получения оксида азота(II) можно использовать прибор, изображённый на рисунке 2.
Другие задания:
Помогло решение? Оставьте отзыв в комментариях ниже.
Мы подготовили для вас ответ c подробным объяснением домашего задания по химии за 10-11 класс, для упражнения номер 180 расположенного на странице 212 к задачнику 2023 года издания для учащихся школ и гимназий.
Теперь на нашем сайте ГДЗ.ТОП вы всегда легко и бесплатно найдёте условие с правильным ответом на вопрос «Как решить ДЗ» и «Как сделать» задание по химии к упражнению №180 (с. 212), авторов: Еремин (Вадим Владимирович), Дроздов (Андрей Анатольевич), Ромашов (Леонид Владимирович), ФГОС (новый, красный) учебного пособия издательства Просвещение.




















