Номер 75, страница 301 - гдз по химии 10-11 класс задачник Еремин, Дроздов

Авторы: Еремин В. В., Дроздов А. А., Ромашов Л. В.
Тип: Задачник
Издательство: Просвещение
Год издания: 2023 - 2025
Цвет обложки: белый, зелёный
ISBN: 978-5-09-109700-9
Популярные ГДЗ в 10 классе
Тема 11. Теоретическое описание химических реакций. 11.2. Энтропия и энергия Гиббса. Химическое равновесие. 11.2.1. Энтропия и энергия Гиббса. Уровень 2 - номер 75, страница 301.
№75 (с. 301)
Условие. №75 (с. 301)
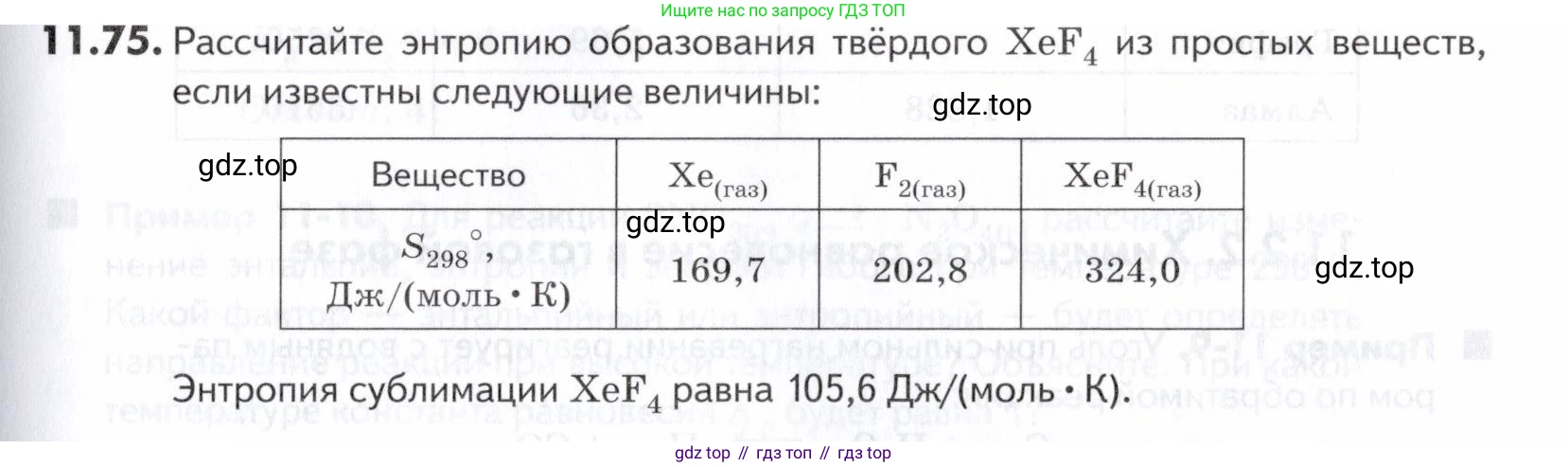
11.75. Рассчитайте энтропию образования твёрдого из простых веществ, если известны следующие величины:
| Вещество | |||
| Дж/(моль • К). | 169,7 | 202,8 | 324,0 |
Энтропия сублимации равна 105,6 Дж/(моль • К).
Решение 3. №75 (с. 301)
Дано:
Стандартная молярная энтропия $S_{298}^{\circ}(Xe_{(\text{газ})}) = 169,7 \text{ Дж/(моль} \cdot \text{К)}$
Стандартная молярная энтропия $S_{298}^{\circ}(F_{2(\text{газ})}) = 202,8 \text{ Дж/(моль} \cdot \text{К)}$
Стандартная молярная энтропия $S_{298}^{\circ}(XeF_{4(\text{газ})}) = 324,0 \text{ Дж/(моль} \cdot \text{К)}$
Энтропия сублимации $XeF_4$, $\Delta_{sub}S^{\circ}(XeF_4) = 105,6 \text{ Дж/(моль} \cdot \text{К)}$
Все данные приведены в системе СИ.
Найти:Энтропию образования твёрдого $XeF_4$, $\Delta_f S^{\circ}(XeF_{4(\text{тв.)}})$
Решение:1. Для расчёта энтропии образования твёрдого $XeF_4$ необходимо знать его стандартную молярную энтропию $S^{\circ}(XeF_{4(\text{тв.)}})$. Мы можем найти эту величину, используя данные об энтропии газообразного $XeF_4$ и энтропии его сублимации (возгонки).
Процесс сублимации описывается уравнением: $XeF_{4(\text{тв.})} \rightarrow XeF_{4(\text{газ})}$
Изменение энтропии для этого фазового перехода равно: $\Delta_{sub}S^{\circ} = S^{\circ}(XeF_{4(\text{газ})}) - S^{\circ}(XeF_{4(\text{тв.)}})$
Выразим отсюда стандартную молярную энтропию твёрдого тетрафторида ксенона:
$S^{\circ}(XeF_{4(\text{тв.)}}) = S^{\circ}(XeF_{4(\text{газ})}) - \Delta_{sub}S^{\circ}$
Подставим числовые значения из условия:
$S^{\circ}(XeF_{4(\text{тв.)}}) = 324,0 \text{ Дж/(моль} \cdot \text{К)} - 105,6 \text{ Дж/(моль} \cdot \text{К)} = 218,4 \text{ Дж/(моль} \cdot \text{К)}$
2. Теперь мы можем рассчитать энтропию образования твёрдого $XeF_4$ из простых веществ. Простые вещества ксенон ($Xe$) и фтор ($F_2$) при стандартных условиях (298 К) являются газами. Реакция образования:
$Xe_{(\text{газ})} + 2F_{2(\text{газ})} \rightarrow XeF_{4(\text{тв.})}$
Энтропия образования ($\Delta_f S^{\circ}$) равна изменению энтропии в этой реакции и вычисляется как разность сумм стандартных энтропий продуктов и реагентов с учётом их стехиометрических коэффициентов:
$\Delta_f S^{\circ} = S^{\circ}(XeF_{4(\text{тв.)}}) - [S^{\circ}(Xe_{(\text{газ})}) + 2 \cdot S^{\circ}(F_{2(\text{газ})})]$
Подставим все известные и вычисленные значения в формулу:
$\Delta_f S^{\circ}(XeF_{4(\text{тв.)}}) = 218,4 - (169,7 + 2 \cdot 202,8)$
$\Delta_f S^{\circ}(XeF_{4(\text{тв.)}}) = 218,4 - (169,7 + 405,6)$
$\Delta_f S^{\circ}(XeF_{4(\text{тв.)}}) = 218,4 - 575,3$
$\Delta_f S^{\circ}(XeF_{4(\text{тв.)}}) = -356,9 \text{ Дж/(моль} \cdot \text{К)}$
Ответ: энтропия образования твёрдого $XeF_4$ из простых веществ равна $-356,9 \text{ Дж/(моль} \cdot \text{К)}$.
Другие задания:
Помогло решение? Оставьте отзыв в комментариях ниже.
Мы подготовили для вас ответ c подробным объяснением домашего задания по химии за 10-11 класс, для упражнения номер 75 расположенного на странице 301 к задачнику 2023 года издания для учащихся школ и гимназий.
Теперь на нашем сайте ГДЗ.ТОП вы всегда легко и бесплатно найдёте условие с правильным ответом на вопрос «Как решить ДЗ» и «Как сделать» задание по химии к упражнению №75 (с. 301), авторов: Еремин (Вадим Владимирович), Дроздов (Андрей Анатольевич), Ромашов (Леонид Владимирович), ФГОС (новый, красный) учебного пособия издательства Просвещение.




















