Номер 94, страница 38 - гдз по химии 10-11 класс задачник Еремин, Дроздов

Авторы: Еремин В. В., Дроздов А. А., Ромашов Л. В.
Тип: Задачник
Издательство: Просвещение
Год издания: 2023 - 2025
Цвет обложки: белый, зелёный
ISBN: 978-5-09-109700-9
Популярные ГДЗ в 10 классе
Тема 2. Углеводороды. 2.2. Углеводороды с двойной связью. Уровень 1 - номер 94, страница 38.
№94 (с. 38)
Условие. №94 (с. 38)

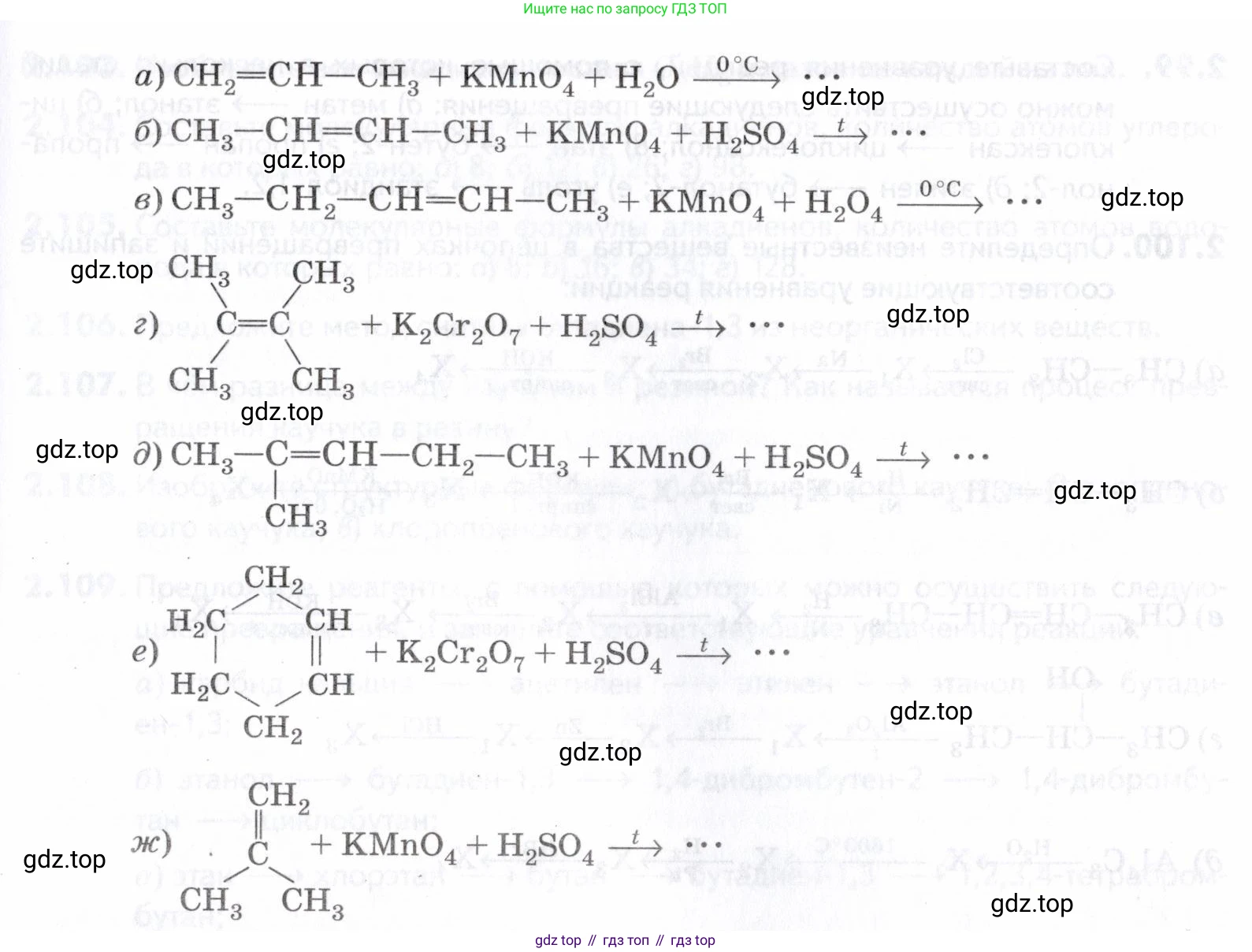
2.94. Определите продукты следующих окислительно-восстановительных реакций и уравняйте их:
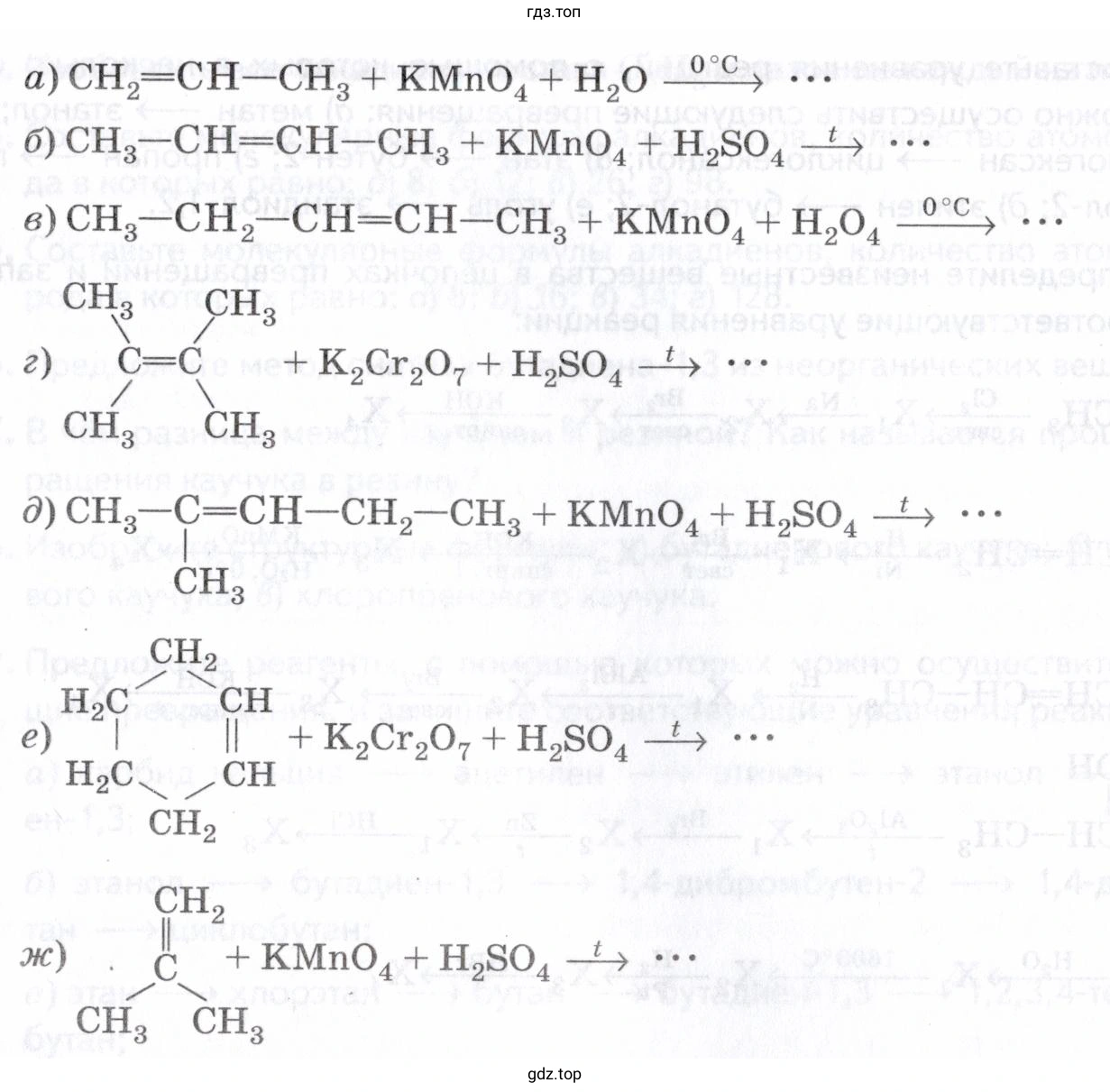
Решение. №94 (с. 38)
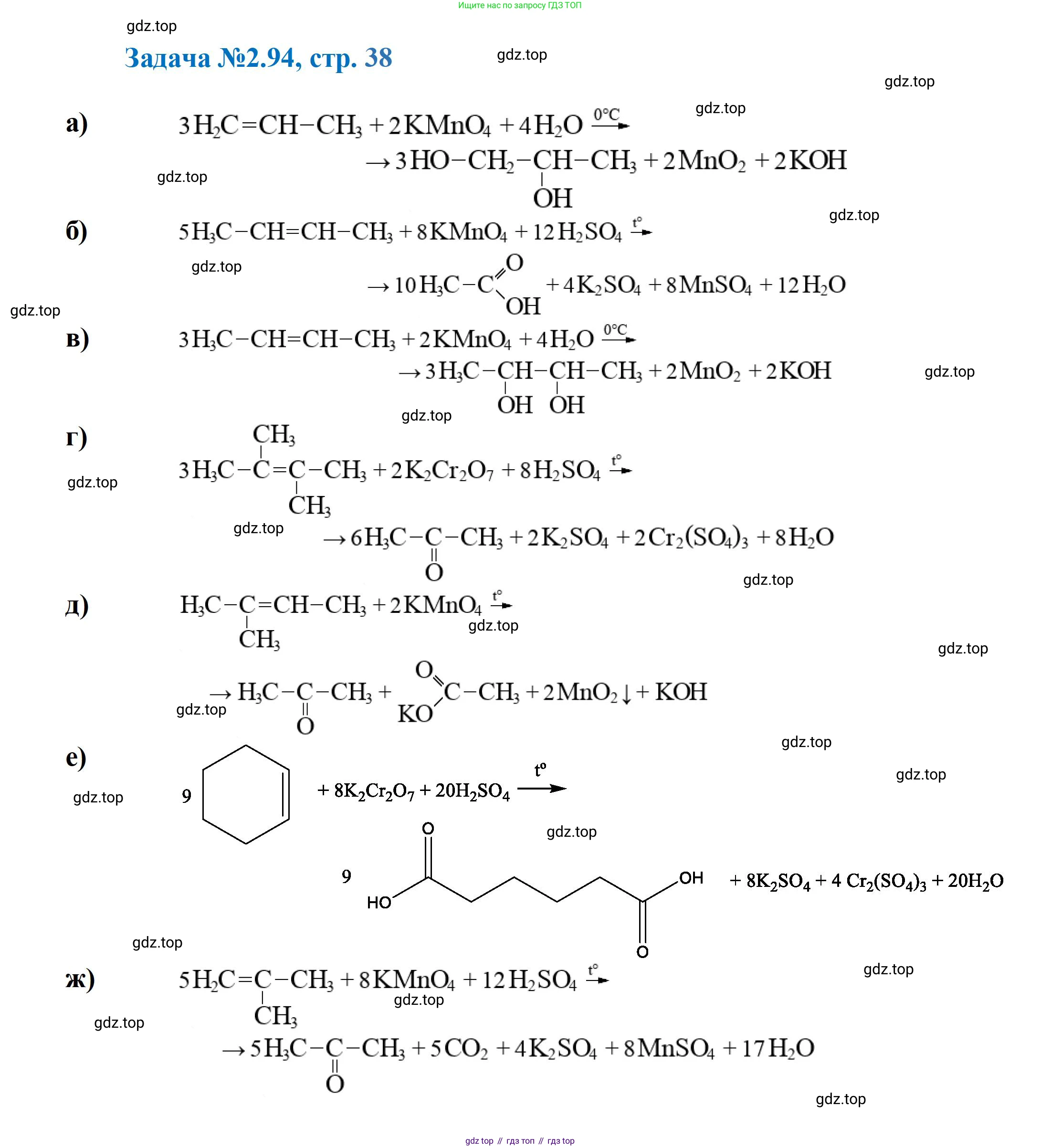
Решение 3. №94 (с. 38)
а) Дано:
Схема реакции: $CH_2=CH-CH_3 + KMnO_4 + H_2O \xrightarrow{0^{\circ}C} ...$
Найти:
Продукты реакции и стехиометрические коэффициенты.
Решение:
Это реакция мягкого окисления пропена водным раствором перманганата калия при низкой температуре (реакция Вагнера). При этих условиях происходит разрыв только $\pi$-связи в двойной связи $C=C$ с образованием двухатомного спирта (гликоля) — пропан-1,2-диола. Марганец в перманганате калия (степень окисления $+7$) восстанавливается до оксида марганца(IV) (степень окисления $+4$), который выпадает в виде бурого осадка.
Составим полуреакции окисления и восстановления, чтобы уравнять реакцию методом электронного баланса:
Окисление (восстановитель — пропен):
$C_3H_6 \rightarrow C_3H_8O_2$
Атомы углерода при двойной связи меняют степень окисления: $C^{-2} \rightarrow C^{-1}$ (отдает 1 электрон) и $C^{-1} \rightarrow C^{0}$ (отдает 1 электрон). Суммарно молекула пропена отдает 2 электрона.
$C_3H_6 - 2e^- \rightarrow C_3H_8O_2$
Восстановление (окислитель — перманганат-ион):
$Mn^{+7} + 3e^- \rightarrow Mn^{+4}$ (в $MnO_2$)
Находим наименьшее общее кратное для чисел электронов (НОК(2, 3) = 6) и расставляем коэффициенты:
$3 | C_3H_6 - 2e^- \rightarrow C_3H_8O_2$
$2 | Mn^{+7} + 3e^- \rightarrow Mn^{+4}$
Подставляем коэффициенты в уравнение реакции и уравниваем остальные элементы (K, O, H):
$3CH_2=CH-CH_3 + 2KMnO_4 + 4H_2O \rightarrow 3CH_3-CH(OH)-CH_2(OH) + 2MnO_2\downarrow + 2KOH$
Ответ:
$3CH_2=CH-CH_3 + 2KMnO_4 + 4H_2O \xrightarrow{0^{\circ}C} 3CH_3-CH(OH)-CH_2(OH) + 2MnO_2\downarrow + 2KOH$
б) Дано:
Схема реакции: $CH_3-CH=CH-CH_3 + KMnO_4 + H_2SO_4 \xrightarrow{t} ...$
Найти:
Продукты реакции и стехиометрические коэффициенты.
Решение:
Это реакция жесткого окисления бут-2-ена в кислой среде при нагревании. Происходит полный разрыв двойной связи ($C=C$). Поскольку оба атома углерода при двойной связи являются вторичными ($R-CH=$), они окисляются до карбоксильных групп ($-COOH$). Таким образом, из одной молекулы бут-2-ена образуются две молекулы уксусной кислоты ($CH_3COOH$). Марганец ($Mn^{+7}$) в кислой среде восстанавливается до $Mn^{+2}$.
Составим полуреакции окисления и восстановления:
Окисление: каждый из двух атомов углерода при двойной связи меняет степень окисления с $-1$ на $+3$, отдавая по 4 электрона. Суммарно молекула отдает 8 электронов.
$CH_3-CH=CH-CH_3 + 4H_2O - 8e^- \rightarrow 2CH_3COOH + 8H^+$
Восстановление:
$MnO_4^- + 8H^+ + 5e^- \rightarrow Mn^{2+} + 4H_2O$
Находим НОК(8, 5) = 40 и расставляем коэффициенты:
$5 | C_4H_8 + 4H_2O - 8e^- \rightarrow 2CH_3COOH + 8H^+$
$8 | MnO_4^- + 8H^+ + 5e^- \rightarrow Mn^{2+} + 4H_2O$
Суммируем ионные уравнения и сокращаем подобные члены:
$5C_4H_8 + 20H_2O + 8MnO_4^- + 64H^+ \rightarrow 10CH_3COOH + 40H^+ + 8Mn^{2+} + 32H_2O$
$5C_4H_8 + 8MnO_4^- + 24H^+ \rightarrow 10CH_3COOH + 8Mn^{2+} + 12H_2O$
Записываем полное молекулярное уравнение:
$5CH_3-CH=CH-CH_3 + 8KMnO_4 + 12H_2SO_4 \rightarrow 10CH_3COOH + 8MnSO_4 + 4K_2SO_4 + 12H_2O$
Ответ:
$5CH_3-CH=CH-CH_3 + 8KMnO_4 + 12H_2SO_4 \xrightarrow{t} 10CH_3COOH + 4K_2SO_4 + 8MnSO_4 + 12H_2O$
в) Дано:
Схема реакции: $CH_3-CH_2-CH=CH-CH=CH-CH_3 + KMnO_4 + H_2O \xrightarrow{0^{\circ}C} ...$ (в условии опечатка $H_2O_4$, имеется в виду $H_2O$)
Найти:
Продукты реакции и стехиометрические коэффициенты.
Решение:
Это реакция мягкого окисления гептадиена-2,4 водным раствором перманганата калия. Окислению подвергаются обе двойные связи. По месту разрыва $\pi$-связей присоединяются гидроксильные группы, образуя четырехатомный спирт — гептантетраол-2,3,4,5. Как и в реакции (а), марганец восстанавливается до $MnO_2$.
Составим электронный баланс. Каждый из четырех атомов углерода при двойных связях ($C^2, C^3, C^4, C^5$) имеет степень окисления $-1$ и окисляется до степени окисления $0$, отдавая по 1 электрону. Суммарно молекула отдает 4 электрона.
Окисление: $C_7H_{12} - 4e^- \rightarrow C_7H_{16}O_4$
Восстановление: $Mn^{+7} + 3e^- \rightarrow Mn^{+4}$
НОК(4, 3) = 12. Расставляем коэффициенты:
$3 | C_7H_{12} - 4e^- \rightarrow C_7H_{16}O_4$
$4 | Mn^{+7} + 3e^- \rightarrow Mn^{+4}$
Подставляем коэффициенты в уравнение и уравниваем:
$3C_7H_{12} + 4KMnO_4 + 8H_2O \rightarrow 3C_7H_{16}O_4 + 4MnO_2\downarrow + 4KOH$
Ответ:
$3CH_3-CH_2-(CH=CH)_2-CH_3 + 4KMnO_4 + 8H_2O \xrightarrow{0^{\circ}C} 3CH_3-CH_2-(CHOH)_4-CH_3 + 4MnO_2\downarrow + 4KOH$
г) Дано:
Схема реакции: $(CH_3)_2C=C(CH_3)_2 + K_2Cr_2O_7 + H_2SO_4 \xrightarrow{t} ...$
Найти:
Продукты реакции и стехиометрические коэффициенты.
Решение:
Это реакция жесткого окисления 2,3-диметилбут-2-ена дихроматом калия в кислой среде. Происходит полный разрыв двойной связи. Оба атома углерода при двойной связи являются третичными ($R_2C=$) и окисляются до кетогрупп. В данном случае из одной молекулы алкена образуются две молекулы ацетона (пропан-2-она). Хром в дихромат-ионе ($Cr_2O_7^{2-}$) имеет степень окисления $+6$ и восстанавливается в кислой среде до $Cr^{+3}$.
Составим полуреакции:
Окисление: оба атома углерода при двойной связи меняют степень окисления с $0$ на $+2$, отдавая по 2 электрона. Суммарно молекула отдает 4 электрона.
$(CH_3)_2C=C(CH_3)_2 + 2H_2O - 4e^- \rightarrow 2(CH_3)_2C=O + 4H^+$
Восстановление: каждый из двух атомов хрома принимает по 3 электрона.
$Cr_2O_7^{2-} + 14H^+ + 6e^- \rightarrow 2Cr^{3+} + 7H_2O$
НОК(4, 6) = 12. Расставляем коэффициенты:
$3 | C_6H_{12} + 2H_2O - 4e^- \rightarrow 2C_3H_6O + 4H^+$
$2 | Cr_2O_7^{2-} + 14H^+ + 6e^- \rightarrow 2Cr^{3+} + 7H_2O$
Суммируем ионные уравнения и сокращаем:
$3C_6H_{12} + 6H_2O + 2Cr_2O_7^{2-} + 28H^+ \rightarrow 6C_3H_6O + 12H^+ + 4Cr^{3+} + 14H_2O$
$3C_6H_{12} + 2Cr_2O_7^{2-} + 16H^+ \rightarrow 6C_3H_6O + 4Cr^{3+} + 8H_2O$
Записываем полное молекулярное уравнение:
$3(CH_3)_2C=C(CH_3)_2 + 2K_2Cr_2O_7 + 8H_2SO_4 \rightarrow 6(CH_3)_2C=O + 2Cr_2(SO_4)_3 + 2K_2SO_4 + 8H_2O$
Ответ:
$3(CH_3)_2C=C(CH_3)_2 + 2K_2Cr_2O_7 + 8H_2SO_4 \xrightarrow{t} 6(CH_3)_2C=O + 2K_2SO_4 + 2Cr_2(SO_4)_3 + 8H_2O$
д) Дано:
Схема реакции: $CH_3-C(CH_3)=CH-CH_2-CH_3 + KMnO_4 + H_2SO_4 \xrightarrow{t} ...$
Найти:
Продукты реакции и стехиометрические коэффициенты.
Решение:
Это реакция жесткого окисления 2-метилпент-2-ена в кислой среде. При разрыве двойной связи третичный атом углерода ($>C=$) окисляется до кетогруппы, а вторичный ($=CH-$) — до карбоксильной группы. Таким образом, образуются ацетон ($(CH_3)_2C=O$) и пропановая кислота ($CH_3CH_2COOH$).
Определим число отданных электронов: $C^2$ (степень окисления $0$) окисляется до $C^{+2}$ в кетоне (отдает 2e-). $C^3$ (степень окисления $-1$) окисляется до $C^{+3}$ в кислоте (отдает 4e-). Суммарно молекула отдает 6 электронов.
Окисление: $C_6H_{12} - 6e^- \rightarrow (CH_3)_2C=O + CH_3CH_2COOH$
Восстановление: $Mn^{+7} + 5e^- \rightarrow Mn^{+2}$
НОК(6, 5) = 30. Расставляем коэффициенты:
$5 | C_6H_{12} - 6e^- \rightarrow C_3H_6O + C_3H_6O_2$
$6 | Mn^{+7} + 5e^- \rightarrow Mn^{+2}$
Подставляем коэффициенты и уравниваем реакцию в молекулярном виде:
$5CH_3-C(CH_3)=CH-CH_2-CH_3 + 6KMnO_4 + 9H_2SO_4 \rightarrow 5(CH_3)_2C=O + 5CH_3CH_2COOH + 3K_2SO_4 + 6MnSO_4 + 9H_2O$
Ответ:
$5CH_3-C(CH_3)=CH-CH_2-CH_3 + 6KMnO_4 + 9H_2SO_4 \xrightarrow{t} 5(CH_3)_2C=O + 5CH_3CH_2COOH + 3K_2SO_4 + 6MnSO_4 + 9H_2O$
е) Дано:
Схема реакции: циклогексен $+ K_2Cr_2O_7 + H_2SO_4 \xrightarrow{t} ...$
Найти:
Продукты реакции и стехиометрические коэффициенты.
Решение:
Это реакция жесткого окисления циклического алкена — циклогексена. При разрыве двойной связи в цикле происходит размыкание кольца. Оба атома углерода при двойной связи являются вторичными, поэтому они окисляются до карбоксильных групп. В результате образуется одна молекула двухосновной карбоновой кислоты — адипиновой кислоты ($HOOC-(CH_2)_4-COOH$).
Составим электронный баланс: два атома углерода при двойной связи ($C^{-1}$) окисляются до карбоксильных атомов углерода ($C^{+3}$), каждый отдает по 4 электрона. Суммарно молекула отдает 8 электронов.
Окисление: $C_6H_{10} - 8e^- \rightarrow C_6H_{10}O_4$ (адипиновая кислота)
Восстановление: $Cr_2O_7^{2-} + 6e^- \rightarrow 2Cr^{3+}$
НОК(8, 6) = 24. Расставляем коэффициенты:
$3 | C_6H_{10} - 8e^- \rightarrow C_6H_{10}O_4$
$4 | Cr_2O_7^{2-} + 6e^- \rightarrow 2Cr^{3+}$
Подставляем коэффициенты и уравниваем полное молекулярное уравнение:
$3C_6H_{10} + 4K_2Cr_2O_7 + 16H_2SO_4 \rightarrow 3HOOC-(CH_2)_4-COOH + 4K_2SO_4 + 4Cr_2(SO_4)_3 + 16H_2O$
Ответ:
$3C_6H_{10} + 4K_2Cr_2O_7 + 16H_2SO_4 \xrightarrow{t} 3HOOC-(CH_2)_4-COOH + 4K_2SO_4 + 4Cr_2(SO_4)_3 + 16H_2O$
ж) Дано:
Схема реакции: $(CH_3)_2C=CH_2 + KMnO_4 + H_2SO_4 \xrightarrow{t} ...$
Найти:
Продукты реакции и стехиометрические коэффициенты.
Решение:
Это реакция жесткого окисления 2-метилпропена (изобутилена) в кислой среде. При разрыве двойной связи третичный атом углерода ($>C=$) окисляется до кетогруппы, образуя ацетон ($(CH_3)_2C=O$). Первичный атом углерода ($=CH_2$) окисляется до углекислого газа ($CO_2$).
Определим число отданных электронов: $C^2$ (степень окисления $0$) окисляется до $C^{+2}$ в кетоне (отдает 2e-). $C^1$ (степень окисления $-2$) окисляется до $C^{+4}$ в $CO_2$ (отдает 6e-). Суммарно молекула отдает 8 электронов.
Окисление: $C_4H_8 - 8e^- \rightarrow (CH_3)_2C=O + CO_2$
Восстановление: $Mn^{+7} + 5e^- \rightarrow Mn^{+2}$
НОК(8, 5) = 40. Расставляем коэффициенты:
$5 | C_4H_8 - 8e^- \rightarrow C_3H_6O + CO_2$
$8 | Mn^{+7} + 5e^- \rightarrow Mn^{+2}$
Подставляем коэффициенты и уравниваем полное молекулярное уравнение:
$5(CH_3)_2C=CH_2 + 8KMnO_4 + 12H_2SO_4 \rightarrow 5(CH_3)_2C=O + 5CO_2\uparrow + 4K_2SO_4 + 8MnSO_4 + 17H_2O$
Ответ:
$5(CH_3)_2C=CH_2 + 8KMnO_4 + 12H_2SO_4 \xrightarrow{t} 5(CH_3)_2C=O + 5CO_2\uparrow + 4K_2SO_4 + 8MnSO_4 + 17H_2O$
Другие задания:
Помогло решение? Оставьте отзыв в комментариях ниже.
Мы подготовили для вас ответ c подробным объяснением домашего задания по химии за 10-11 класс, для упражнения номер 94 расположенного на странице 38 к задачнику 2023 года издания для учащихся школ и гимназий.
Теперь на нашем сайте ГДЗ.ТОП вы всегда легко и бесплатно найдёте условие с правильным ответом на вопрос «Как решить ДЗ» и «Как сделать» задание по химии к упражнению №94 (с. 38), авторов: Еремин (Вадим Владимирович), Дроздов (Андрей Анатольевич), Ромашов (Леонид Владимирович), ФГОС (новый, красный) учебного пособия издательства Просвещение.




















