Номер 105, страница 25 - гдз по химии 10-11 класс задачник Еремин, Дроздов

Авторы: Еремин В. В., Дроздов А. А., Ромашов Л. В.
Тип: Задачник
Издательство: Просвещение
Год издания: 2023 - 2025
Цвет обложки: белый, зелёный
ISBN: 978-5-09-109700-9
Популярные ГДЗ в 10 классе
Тема 1. Основные понятия органической химии. 1.3. Электронное строение атома углерода. Электронные эффекты в органической химии. Уровень 2 - номер 105, страница 25.
№105 (с. 25)
Условие. №105 (с. 25)
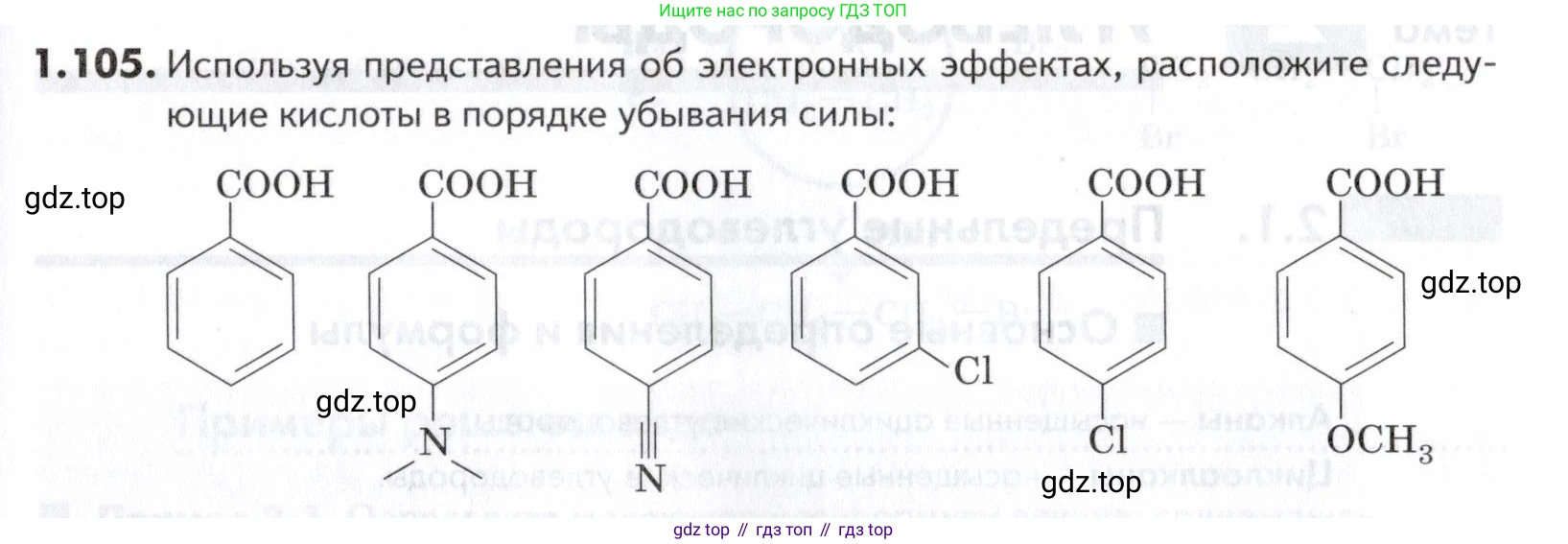
1.105. Используя представления об электронных эффектах, расположите следующие кислоты в порядке убывания силы:
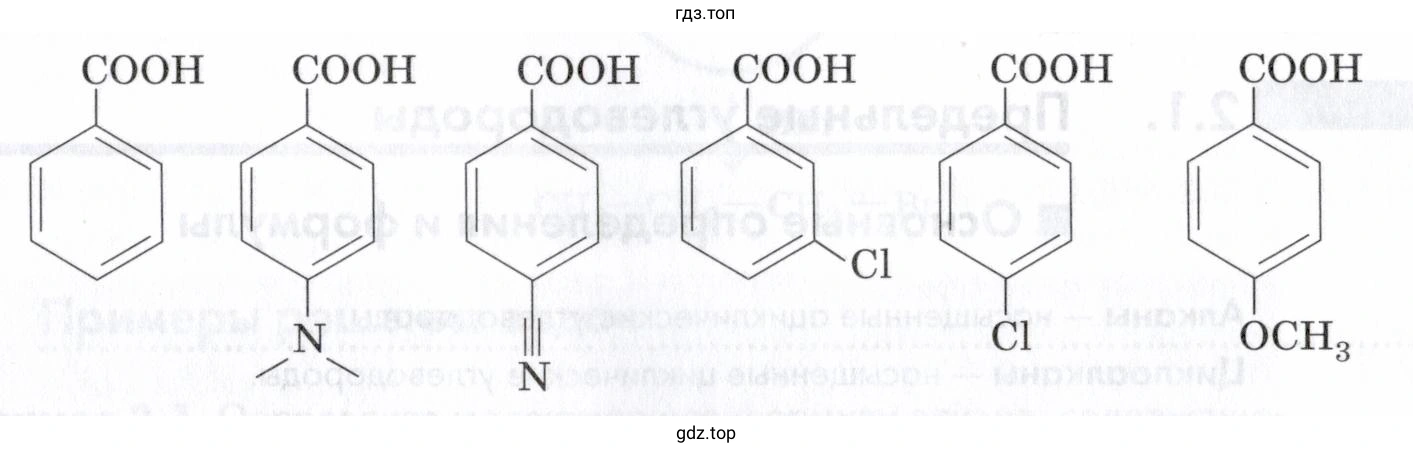
Решение. №105 (с. 25)
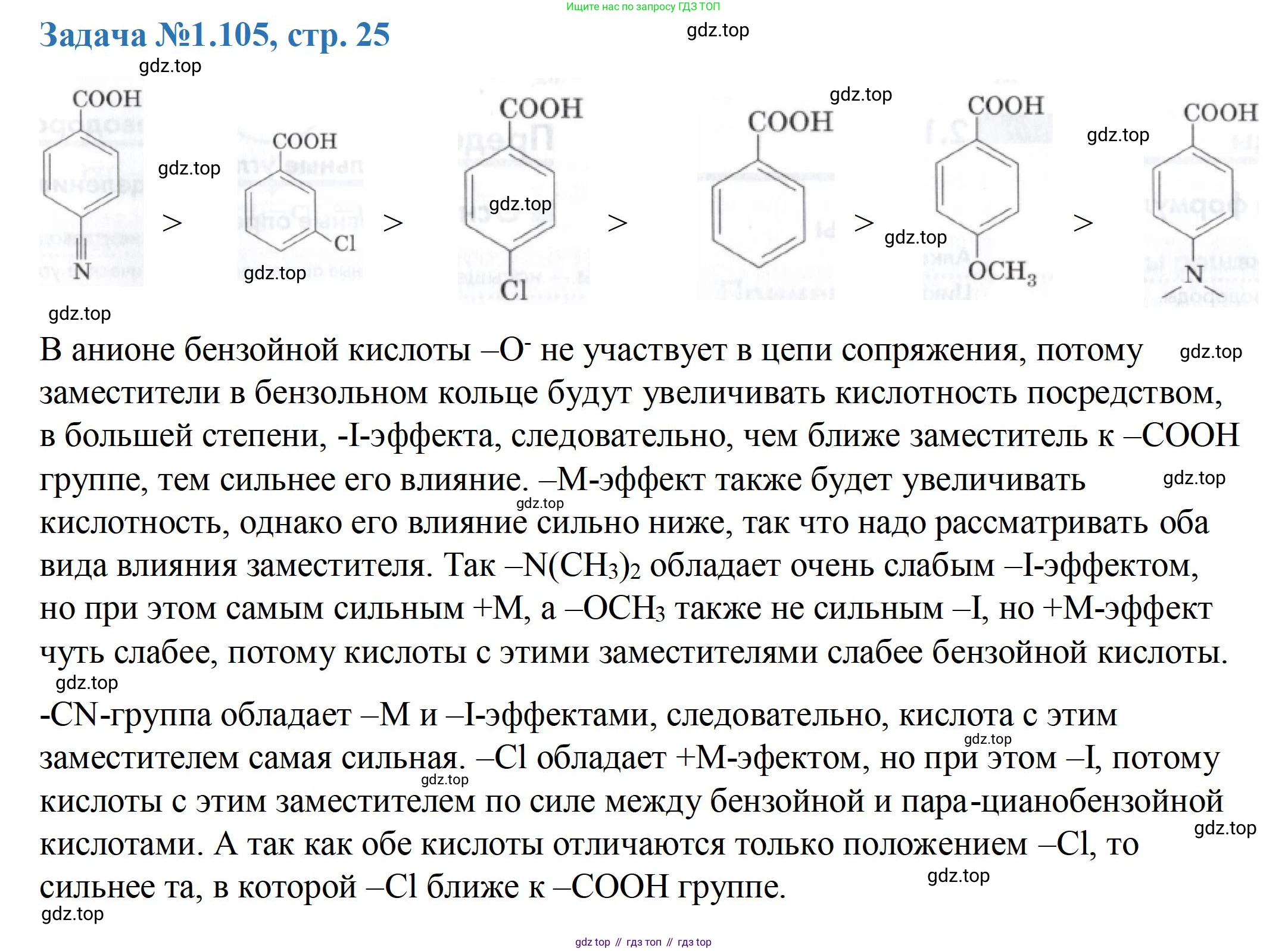
Решение 3. №105 (с. 25)
Решение
Сила карбоновых кислот определяется стабильностью их сопряженного основания — карбоксилат-аниона ($R-COO^-$). Чем стабильнее анион, тем сильнее кислота. Стабильность аниона, в свою очередь, зависит от электронных эффектов заместителей в бензольном кольце.
- Электроноакцепторные группы (ЭАГ) оттягивают электронную плотность от карбоксилатной группы, делокализуя (рассредотачивая) отрицательный заряд. Это стабилизирует анион и, следовательно, увеличивает силу кислоты.
- Электронодонорные группы (ЭДГ) поставляют электронную плотность к карбоксилатной группе, концентрируя на ней отрицательный заряд. Это дестабилизирует анион и уменьшает силу кислоты.
Рассмотрим электронные эффекты заместителей в каждой из представленных кислот. Электронные эффекты делятся на индуктивные ($I$) и мезомерные ($M$).
Далее кислоты проанализированы в порядке убывания их силы.
1. 4-цианобензойная кислота (третья слева).
Цианогруппа ($-CN$) является сильной электроноакцепторной группой. Она проявляет сильный отрицательный индуктивный ($-I$) и сильный отрицательный мезомерный ($-M$) эффекты. Оба эффекта направлены на оттягивание электронов от кольца, что приводит к максимальной стабилизации карбоксилат-аниона в данном ряду. Следовательно, это самая сильная кислота.
2. 3-хлорбензойная кислота (четвертая слева).
Атом хлора ($-Cl$) проявляет сильный $-I$ эффект (из-за высокой электроотрицательности) и слабый положительный мезомерный ($+M$) эффект (за счет неподеленных электронных пар). В мета-положении мезомерный эффект не передается на атом углерода, связанный с карбоксильной группой. Поэтому доминирует сильный $-I$ эффект, который стабилизирует анион и увеличивает кислотность.
3. 4-хлорбензойная кислота (пятая слева).
В пара-положении атом хлора также проявляет $-I$ и $+M$ эффекты. Индуктивный эффект с расстоянием ослабевает, поэтому он слабее, чем из мета-положения. При этом донорный $+M$ эффект частично компенсирует акцепторный $-I$ эффект. Суммарный эффект остается акцепторным (для галогенов $-I > +M$), но он слабее, чем у 3-хлорбензойной кислоты. Поэтому эта кислота слабее 3-хлорбензойной, но сильнее бензойной.
4. Бензойная кислота (первая слева).
Это эталонное соединение в данном ряду, не имеющее заместителей (кроме атома водорода), влияющих на кислотность. Ее сила будет промежуточной между кислотами с ЭАГ и ЭДГ.
5. 4-метоксибензойная кислота (шестая слева).
Метоксигруппа ($-OCH_3$) проявляет $-I$ эффект (из-за электроотрицательности кислорода) и сильный $+M$ эффект. Положительный мезомерный эффект преобладает над индуктивным ($-I < +M$), поэтому группа в целом является электронодонорной. Она повышает электронную плотность в кольце, дестабилизирует карбоксилат-анион и уменьшает кислотность по сравнению с бензойной кислотой.
6. 4-(диметиламино)бензойная кислота (вторая слева).
Диметиламиногруппа ($-N(CH_3)_2$) является очень сильным электронодонорным заместителем. Ее $+M$ эффект значительно сильнее $-I$ эффекта (и сильнее, чем у метоксигруппы, так как азот менее электроотрицателен, чем кислород, и легче отдает свою электронную пару). Эта группа сильно дестабилизирует сопряженное основание, что делает эту кислоту самой слабой в представленном ряду.
Таким образом, кислоты в порядке убывания их силы располагаются следующим образом:
4-цианобензойная кислота > 3-хлорбензойная кислота > 4-хлорбензойная кислота > бензойная кислота > 4-метоксибензойная кислота > 4-(диметиламино)бензойная кислота.
Ответ:
Порядок убывания силы кислот (слева направо - от самой сильной к самой слабой):
Другие задания:
Помогло решение? Оставьте отзыв в комментариях ниже.
Мы подготовили для вас ответ c подробным объяснением домашего задания по химии за 10-11 класс, для упражнения номер 105 расположенного на странице 25 к задачнику 2023 года издания для учащихся школ и гимназий.
Теперь на нашем сайте ГДЗ.ТОП вы всегда легко и бесплатно найдёте условие с правильным ответом на вопрос «Как решить ДЗ» и «Как сделать» задание по химии к упражнению №105 (с. 25), авторов: Еремин (Вадим Владимирович), Дроздов (Андрей Анатольевич), Ромашов (Леонид Владимирович), ФГОС (новый, красный) учебного пособия издательства Просвещение.




















