Номер 101, страница 24 - гдз по химии 10-11 класс задачник Еремин, Дроздов

Авторы: Еремин В. В., Дроздов А. А., Ромашов Л. В.
Тип: Задачник
Издательство: Просвещение
Год издания: 2023 - 2025
Цвет обложки: белый, зелёный
ISBN: 978-5-09-109700-9
Популярные ГДЗ в 10 классе
Тема 1. Основные понятия органической химии. 1.3. Электронное строение атома углерода. Электронные эффекты в органической химии. Уровень 2 - номер 101, страница 24.
№101 (с. 24)
Условие. №101 (с. 24)
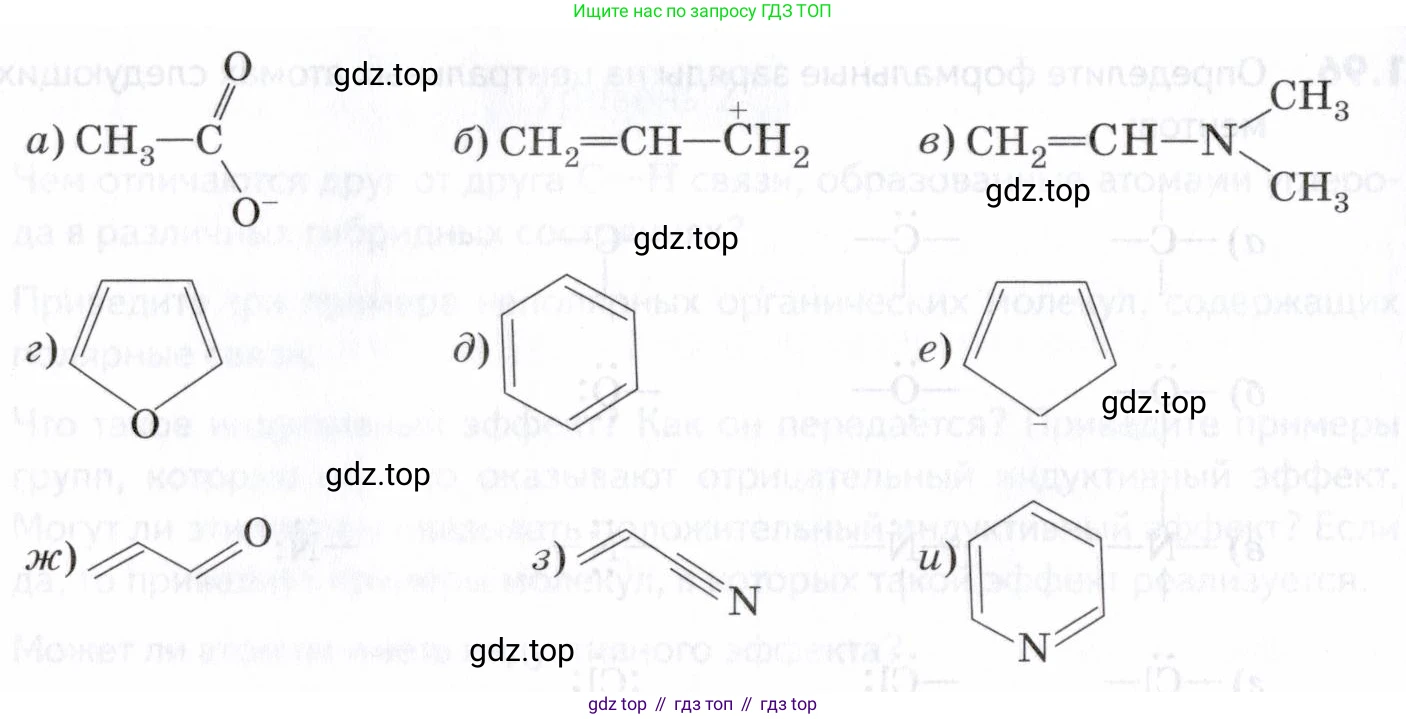
1.101. Изобразите резонансные структуры для следующих частиц:

Решение. №101 (с. 24)
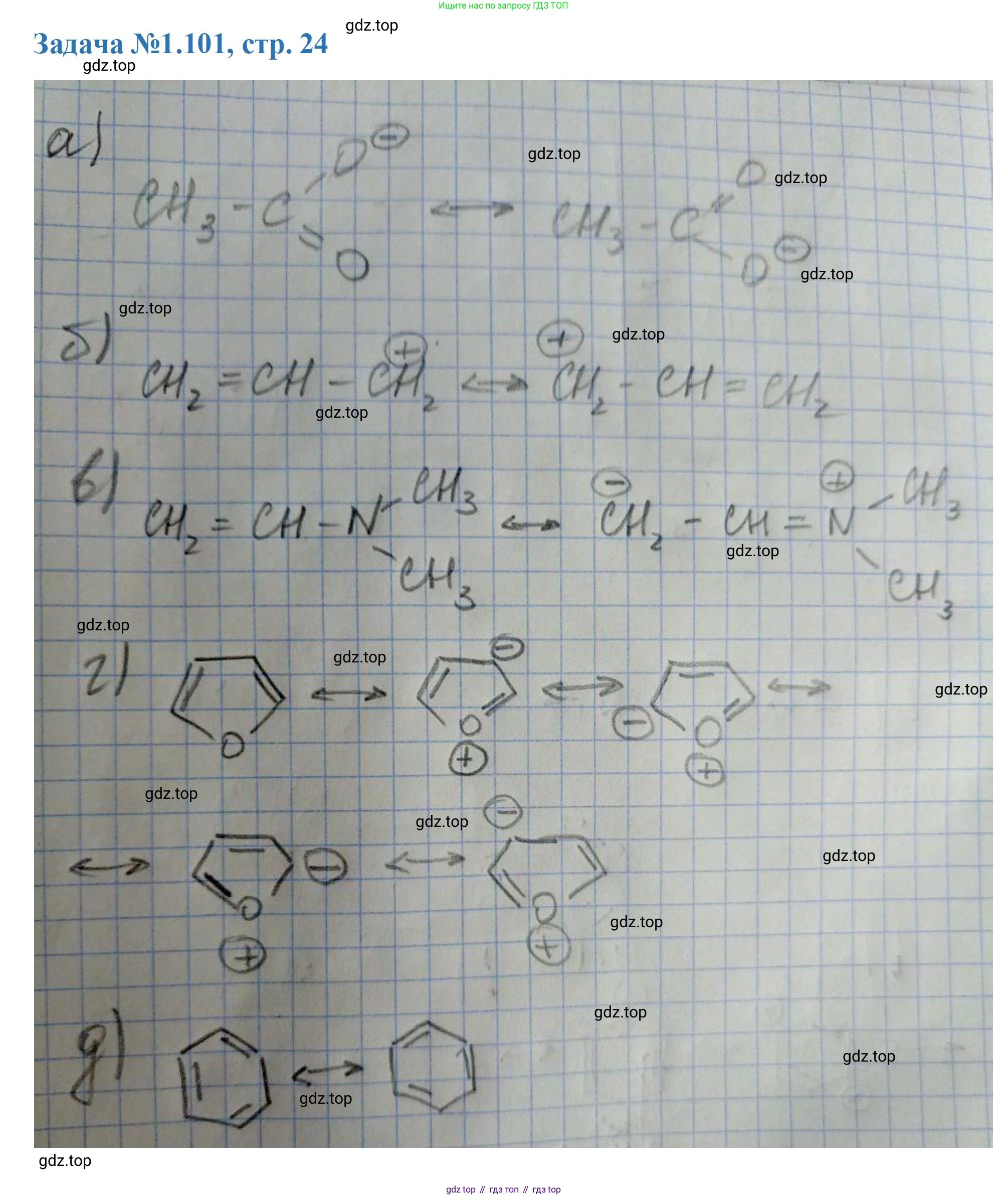
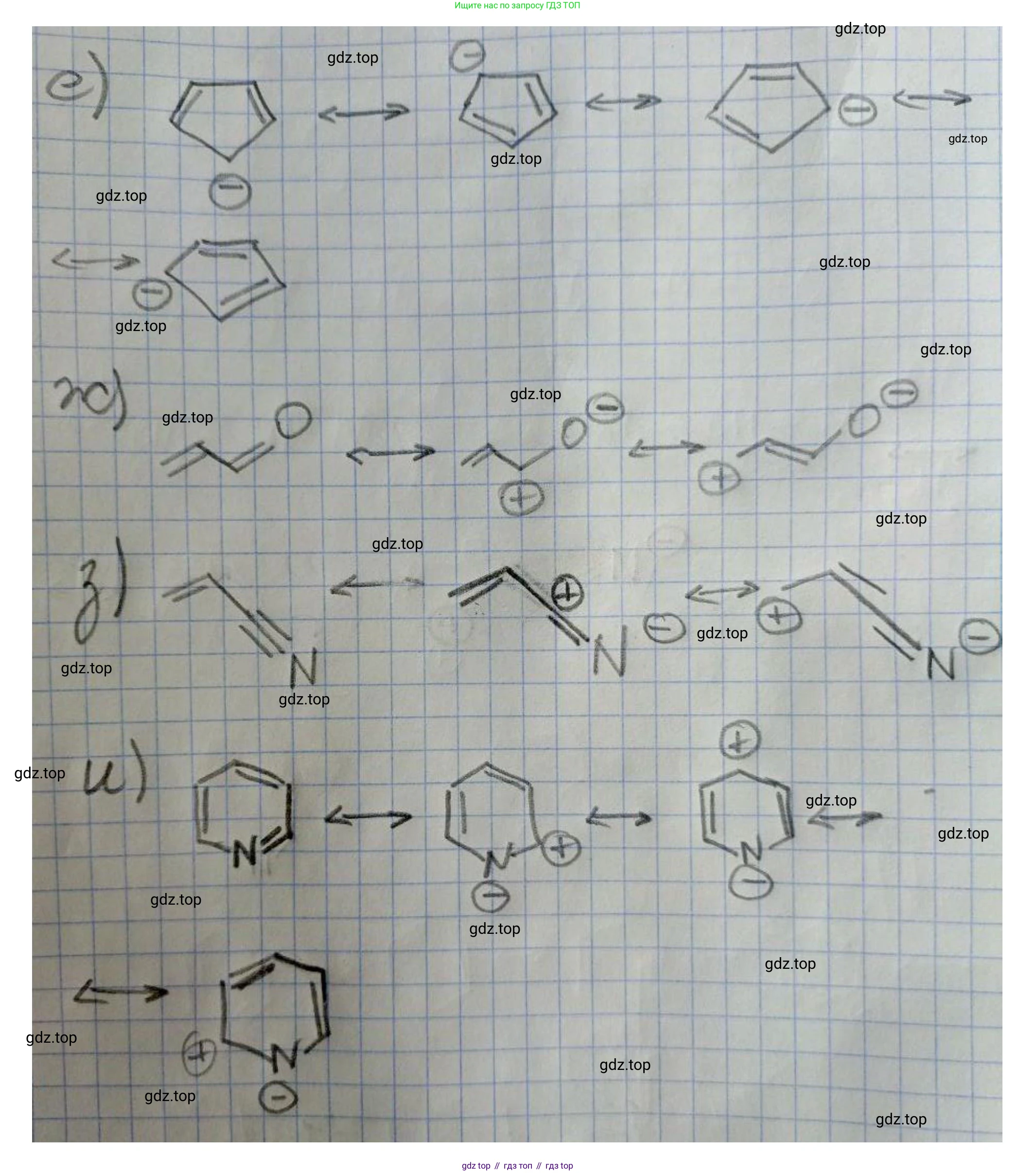
Решение 3. №101 (с. 24)
a) CH₃-C(O)O⁻ (ацетат-ион)
Решение
Ацетат-ион ($CH_3COO^−$) имеет две эквивалентные резонансные структуры. Отрицательный заряд делокализован (распределен) между двумя атомами кислорода. Это происходит за счет сопряжения неподеленной электронной пары отрицательно заряженного атома кислорода с π-электронами двойной связи C=O.
$ \Large \begin{array}{ccc} & \text{:Ö:} & \\ & \| & \\ \text{H}_3\text{C}-\text{C} - \ddot{\text{O}}\text{:}^- \end{array} \leftrightarrow \begin{array}{ccc} & \ddot{\text{O}}\text{:}^- & \\ & | & \\ \text{H}_3\text{C}-\text{C} = \text{:Ö:} \end{array} $
Ответ: Две эквивалентные резонансные структуры, показанные выше, в которых отрицательный заряд распределен между двумя атомами кислорода.
б) CH₂=CH-CH₂⁺ (аллил-катион)
Решение
В аллил-катионе ($CH_2=CH-CH_2^+$) имеется вакантная p-орбиталь у положительно заряженного атома углерода, которая сопряжена с π-системой двойной связи. В результате делокализации π-электронов положительный заряд распределяется между двумя крайними атомами углерода.
$ \Large \text{H}_2\text{C}=\text{CH}-\overset{+}{\text{C}}\text{H}_2 \leftrightarrow \overset{+}{\text{C}}\text{H}_2-\text{CH}=\text{CH}_2 $
Ответ: Две резонансные структуры, показанные выше, с делокализацией положительного заряда по концам аллильной системы.
в) CH₂=CH-N(CH₃)₂ (N,N-диметиламиноэтен)
Решение
В молекуле N,N-диметиламиноэтена неподеленная электронная пара атома азота сопряжена с π-системой двойной связи. Это приводит к возникновению резонансной структуры с разделением зарядов, в которой на атоме азота возникает положительный заряд, а на крайнем атоме углерода — отрицательный (проявление +M-эффекта аминогруппы).
$ \Large \text{H}_2\text{C}=\text{CH}-\ddot{\text{N}}(\text{CH}_3)_2 \leftrightarrow \overset{-}{\text{C}}\text{H}_2-\text{CH}=\overset{+}{\text{N}}(\text{CH}_3)_2 $
Ответ: Две резонансные структуры, одна нейтральная и одна цвиттер-ионная (с разделенными зарядами), как показано выше.
г) Фуран
Решение
Фуран является ароматическим гетероциклом. Его ароматичность обусловлена наличием сопряженной системы из 6 π-электронов в пятичленном цикле (4 электрона от двух связей C=C и 2 электрона от одной из неподеленных пар атома кислорода). Делокализация этих электронов приводит к появлению нескольких резонансных структур. Помимо нейтральной структуры (I), существуют структуры с разделением зарядов (II-V), где атом кислорода несет положительный заряд, а один из атомов углерода – отрицательный.
Ответ: Пять резонансных структур: одна нейтральная (I) и четыре с разделением зарядов (II-V), где отрицательный заряд последовательно находится на каждом из четырех атомов углерода.
д) Бензол
Решение
Бензол — классический пример ароматического соединения с полностью делокализованными π-электронами. Его структура представляет собой резонансный гибрид двух эквивалентных структур Кекуле, в которых формально меняется положение двойных и одинарных связей в шестичленном цикле.
Ответ: Две эквивалентные резонансные структуры Кекуле, показанные выше.
е) Циклопентадиенил-анион
Решение
Циклопентадиенил-анион является ароматической частицей, так как содержит 6 π-электронов в циклической сопряженной системе (4 электрона от двух двойных связей и 2 электрона от неподеленной пары углерода), что удовлетворяет правилу Хюккеля (4n+2 при n=1). Отрицательный заряд равномерно делокализован по всем пяти атомам углерода в цикле, что приводит к пяти эквивалентным резонансным структурам.
Ответ: Пять эквивалентных резонансных структур, в которых отрицательный заряд распределен по всем пяти атомам углерода цикла.
ж) CH₂=CH-CHO (акролеин)
Решение
В молекуле акролеина (пропеналь) имеется сопряженная система, образованная двойной связью C=C и карбонильной группой C=O. Вследствие большей электроотрицательности кислорода, π-электронная плотность смещается к нему. Это отражается во второй резонансной структуре с разделением зарядов, где на атоме кислорода возникает отрицательный заряд, а на крайнем β-атоме углерода — положительный (проявление -M-эффекта альдегидной группы).
$ \Large \text{H}_2\text{C}=\text{CH}-\text{CH}=\ddot{\text{O}} \leftrightarrow \overset{+}{\text{C}}\text{H}_2-\text{CH}=\text{CH}-\text{:\ddot{O}:}^- $
Ответ: Две резонансные структуры: нейтральная и цвиттер-ионная, как показано выше.
з) CH₂=CH-C≡N (акрилонитрил)
Решение
В молекуле акрилонитрила сопряжены двойная связь C=C и тройная связь C≡N нитрильной группы. Атом азота более электроотрицателен, чем углерод, и стягивает на себя электронную плотность из сопряженной системы. Резонансная структура с разделением зарядов показывает положительный заряд на крайнем β-атоме углерода и отрицательный заряд на атоме азота (проявление -M-эффекта нитрильной группы).
$ \Large \text{H}_2\text{C}=\text{CH}-\text{C}\equiv\text{N:} \leftrightarrow \overset{+}{\text{C}}\text{H}_2-\text{CH}=\text{C}=\ddot{\text{N}}\text{:}^- $
Ответ: Две резонансные структуры: нейтральная и цвиттер-ионная, как показано выше.
и) Пиридин
Решение
Пиридин — это ароматический гетероцикл, изоэлектронный аналог бензола. Основными резонансными структурами являются две структуры типа Кекуле (I, II). Однако, из-за высокой электроотрицательности атома азота, он оттягивает электронную плотность из кольца. Это можно изобразить с помощью дополнительных резонансных структур с разделением зарядов (III-V), в которых на атоме азота локализован отрицательный заряд, а на атомах углерода в орто- (C2, C6) и пара- (C4) положениях — положительный. Эти структуры имеют меньший вклад в общую структуру, но важны для объяснения реакционной способности пиридина.
Ответ: Пять резонансных структур: две основные структуры Кекуле (I, II) и три второстепенные цвиттер-ионные структуры (III-V), показанные выше.
Другие задания:
Помогло решение? Оставьте отзыв в комментариях ниже.
Мы подготовили для вас ответ c подробным объяснением домашего задания по химии за 10-11 класс, для упражнения номер 101 расположенного на странице 24 к задачнику 2023 года издания для учащихся школ и гимназий.
Теперь на нашем сайте ГДЗ.ТОП вы всегда легко и бесплатно найдёте условие с правильным ответом на вопрос «Как решить ДЗ» и «Как сделать» задание по химии к упражнению №101 (с. 24), авторов: Еремин (Вадим Владимирович), Дроздов (Андрей Анатольевич), Ромашов (Леонид Владимирович), ФГОС (новый, красный) учебного пособия издательства Просвещение.




















