Номер 95, страница 22 - гдз по химии 10-11 класс задачник Еремин, Дроздов

Авторы: Еремин В. В., Дроздов А. А., Ромашов Л. В.
Тип: Задачник
Издательство: Просвещение
Год издания: 2023 - 2025
Цвет обложки: белый, зелёный
ISBN: 978-5-09-109700-9
Популярные ГДЗ в 10 классе
Тема 1. Основные понятия органической химии. 1.3. Электронное строение атома углерода. Электронные эффекты в органической химии. Уровень 2 - номер 95, страница 22.
№95 (с. 22)
Условие. №95 (с. 22)
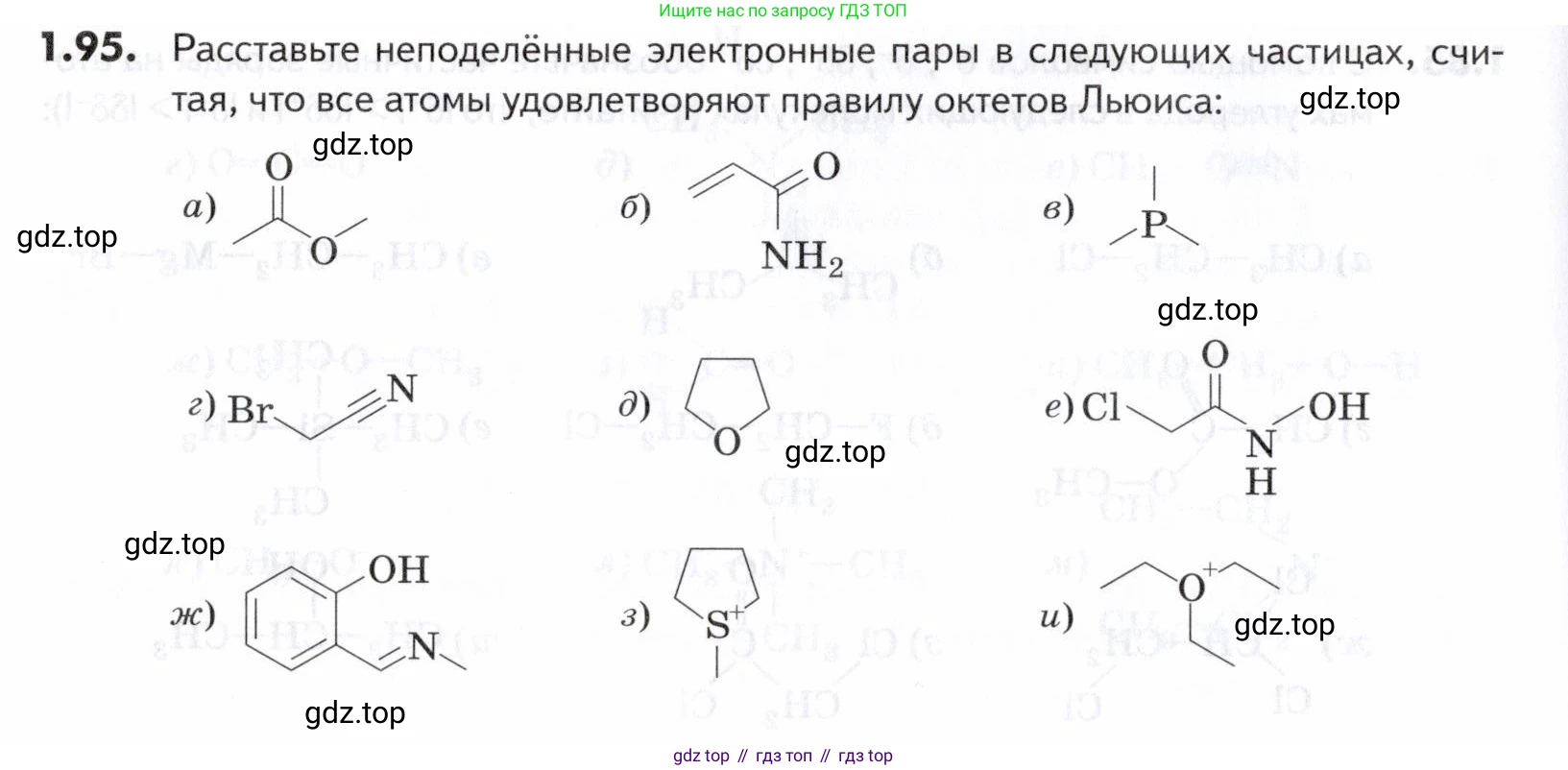

1.95. Расставьте неподелённые электронные пары в следующих частицах, считая, что все атомы удовлетворяют правилу октетов Льюиса:
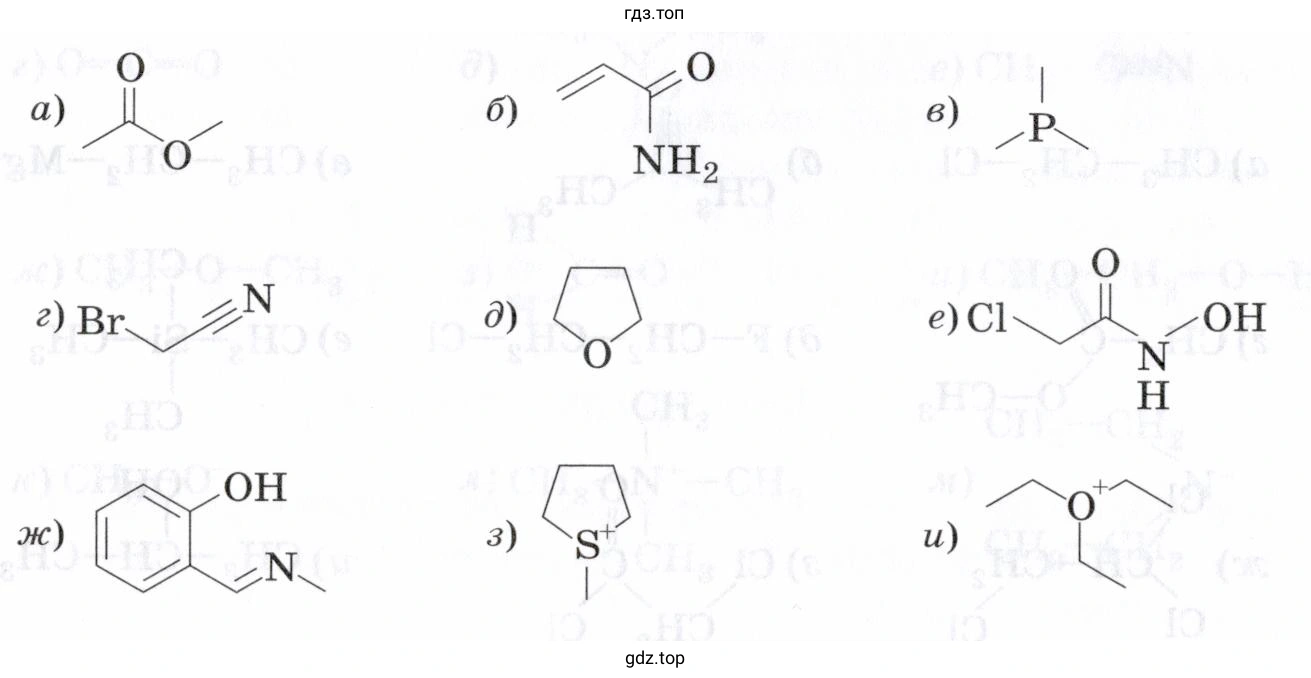
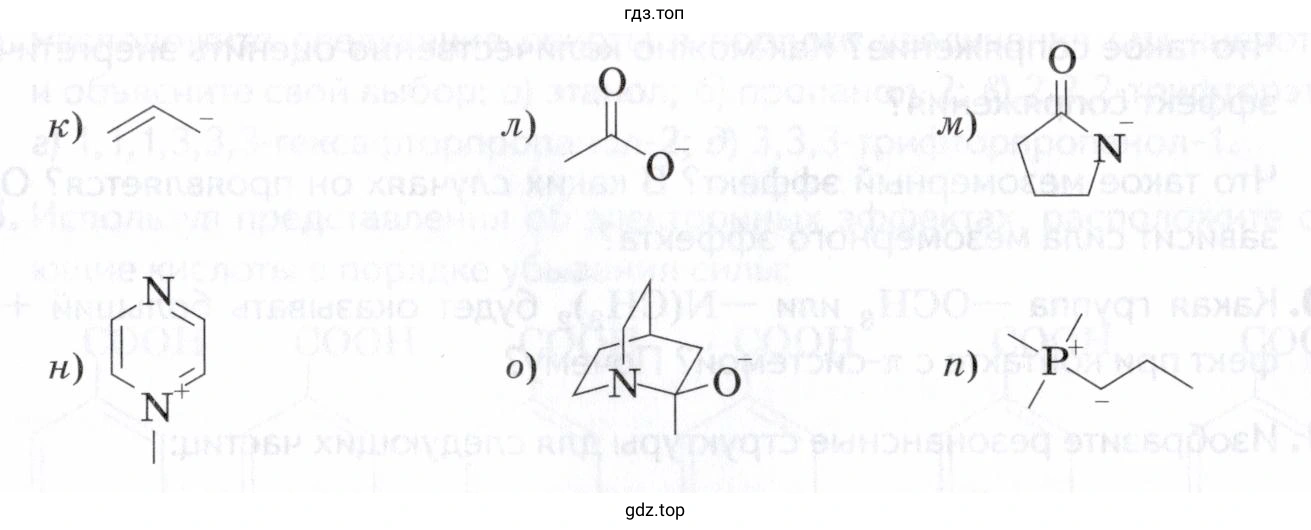
Решение. №95 (с. 22)
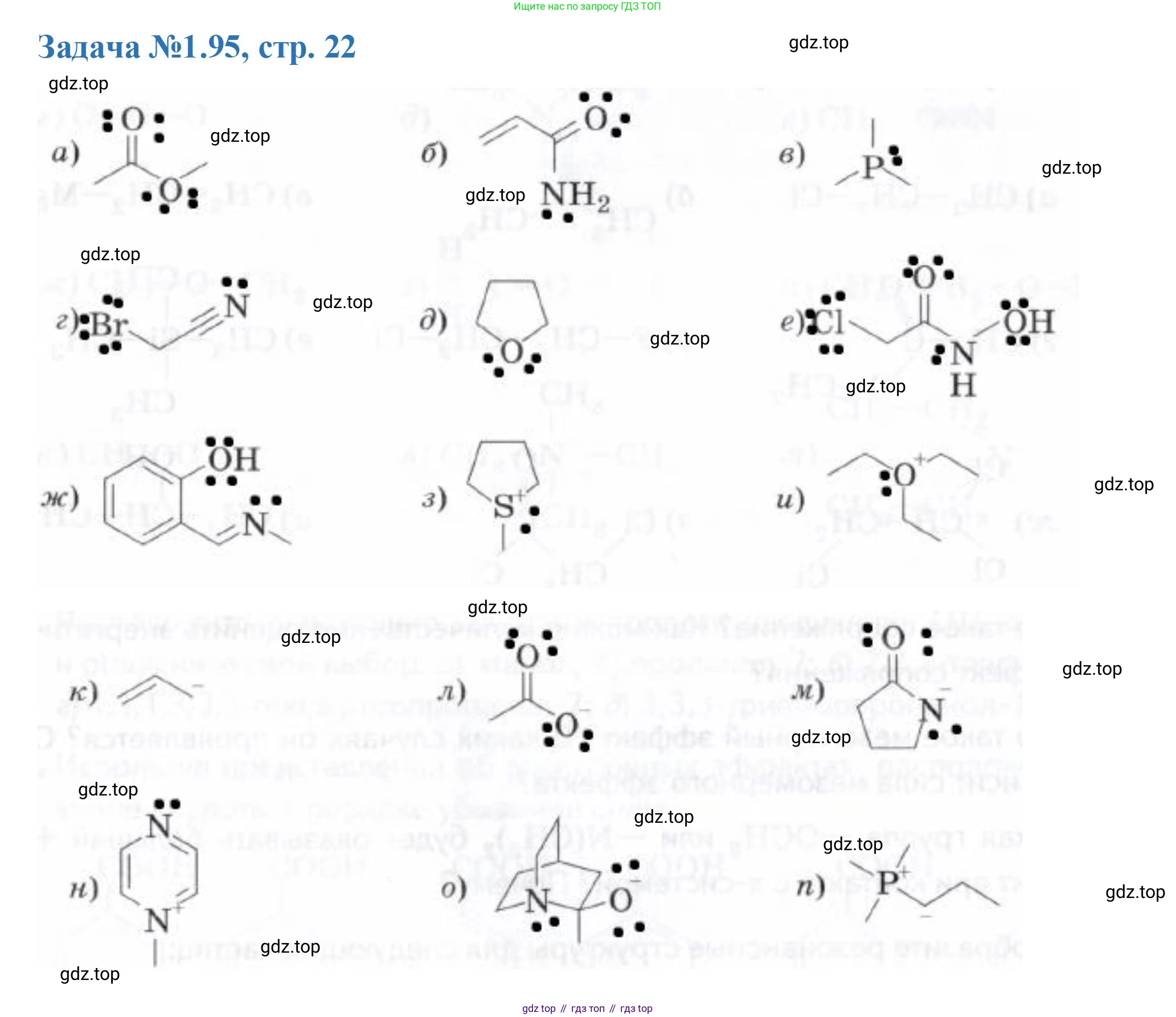
Решение 3. №95 (с. 22)
Решение
Для расстановки неподеленных электронных пар в представленных частицах воспользуемся правилом октетов Льюиса. Согласно этому правилу, атомы элементов (кроме водорода) стремятся к завершению своей валентной оболочки до 8 электронов (как у благородных газов) за счет образования ковалентных связей и неподеленных электронных пар. Число электронов в неподеленных парах для каждого атома определяется так, чтобы общее число электронов (связывающих и неподеленных) вокруг него равнялось восьми.
а) В молекуле метилацетата $CH_3C(O)OCH_3$ есть два атома кислорода. Атом кислорода находится в 16-й группе и имеет 6 валентных электронов.
1. Карбонильный кислород ($O=C$): образует двойную связь с углеродом (4 связывающих электрона). Для выполнения правила октета ему необходимо $8 - 4 = 4$ неподеленных электрона, что составляет 2 неподеленные пары.
2. Эфирный кислород ($C-O-C$): образует две одинарные связи (всего 4 связывающих электрона). Для октета ему необходимо $8 - 4 = 4$ неподеленных электрона, что составляет 2 неподеленные пары.
Ответ:
б) В молекуле акриламида $CH_2=CHCONH_2$ неподеленные пары имеют атомы кислорода и азота.
1. Кислород ($O=C$): Атом кислорода (6 валентных электронов) образует двойную связь. Для октета ему необходимо 2 неподеленные пары (4 электрона).
2. Азот ($N$): Атом азота (5 валентных электронов) образует три одинарные связи (с $C$ и двумя $H$). Он использует 3 валентных электрона. Для октета ему необходимо $8 - (3 \\times 2) = 2$ неподеленных электрона, что составляет 1 неподеленную пару.
Ответ:
в) В молекуле этилдиметилфосфина $CH_3CH_2P(CH_3)_2$ атом фосфора находится в 15-й группе и имеет 5 валентных электронов. Он образует три одинарные связи с атомами углерода, используя 3 своих электрона. Для завершения октета ему необходимо $8 - (3 \\times 2) = 2$ неподеленных электрона, что составляет 1 неподеленную пару.
Ответ:
г) В молекуле бромциана (цианбромида) $Br-C≡N$ неподеленные пары есть у атомов брома и азота.
1. Бром ($Br$): Атом галогена (17-я группа) имеет 7 валентных электронов. Он образует одну одинарную связь, используя 1 электрон. Для октета ему необходимо $8 - 2 = 6$ неподеленных электронов, то есть 3 неподеленные пары.
2. Азот ($N$): Атом азота (15-я группа) имеет 5 валентных электронов. Он образует тройную связь с углеродом (6 связывающих электронов). Для октета ему необходимо $8 - 6 = 2$ неподеленных электрона, то есть 1 неподеленная пара.
Ответ:
д) В молекуле тетрагидрофурана (ТГФ) атом кислорода (6 валентных электронов) в цикле образует две одинарные связи с атомами углерода. Он использует 2 валентных электрона. Для октета ему необходимо $8 - (2 \\times 2) = 4$ неподеленных электрона, что составляет 2 неподеленные пары.
Ответ:
е) В молекуле $N$-гидрокси-2-хлорацетамида $ClCH_2C(O)NH(OH)$ неподеленные пары есть у атомов хлора, двух атомов кислорода и атома азота.
1. Хлор ($Cl$): 7 валентных электронов, 1 одинарная связь. Необходимо 3 неподеленные пары.
2. Карбонильный кислород ($O=C$): 6 валентных электронов, 1 двойная связь. Необходимо 2 неподеленные пары.
3. Азот ($N$): 5 валентных электронов, 3 одинарные связи. Необходима 1 неподеленная пара.
4. Гидроксильный кислород ($O-H$): 6 валентных электронов, 2 одинарные связи. Необходимо 2 неподеленные пары.
Ответ:
ж) В молекуле $2-((метилимино)метил)фенола$ неподеленные пары имеют атом кислорода и атом азота.
1. Кислород ($O$): 6 валентных электронов, 2 одинарные связи (с $C$ и $H$). Необходимо 2 неподеленные пары.
2. Азот ($N$): 5 валентных электронов, 1 двойная связь с $C$ и 1 одинарная связь с $C$. Использует 3 валентных электрона. Необходима 1 неподеленная пара.
Ответ:
з) В катионе 1-метилтиолания атом серы имеет положительный заряд $S^+$. Сера находится в 16-й группе (6 валентных электронов). Положительный заряд означает потерю одного электрона, поэтому для распределения остаются 5 электронов. Атом серы
Другие задания:
Помогло решение? Оставьте отзыв в комментариях ниже.
Мы подготовили для вас ответ c подробным объяснением домашего задания по химии за 10-11 класс, для упражнения номер 95 расположенного на странице 22 к задачнику 2023 года издания для учащихся школ и гимназий.
Теперь на нашем сайте ГДЗ.ТОП вы всегда легко и бесплатно найдёте условие с правильным ответом на вопрос «Как решить ДЗ» и «Как сделать» задание по химии к упражнению №95 (с. 22), авторов: Еремин (Вадим Владимирович), Дроздов (Андрей Анатольевич), Ромашов (Леонид Владимирович), ФГОС (новый, красный) учебного пособия издательства Просвещение.




















