Номер 19, страница 252 - гдз по химии 10-11 класс задачник Еремин, Дроздов

Авторы: Еремин В. В., Дроздов А. А., Ромашов Л. В.
Тип: Задачник
Издательство: Просвещение
Год издания: 2023 - 2025
Цвет обложки: белый, зелёный
ISBN: 978-5-09-109700-9
Популярные ГДЗ в 10 классе
Тема 10. Строение вещества. 10.1. Строение атома и Периодический закон. 10.1.1. Ядро атома. Изотопы. Ядерные реакции. Уровень 1 - номер 19, страница 252.
№19 (с. 252)
Условие. №19 (с. 252)
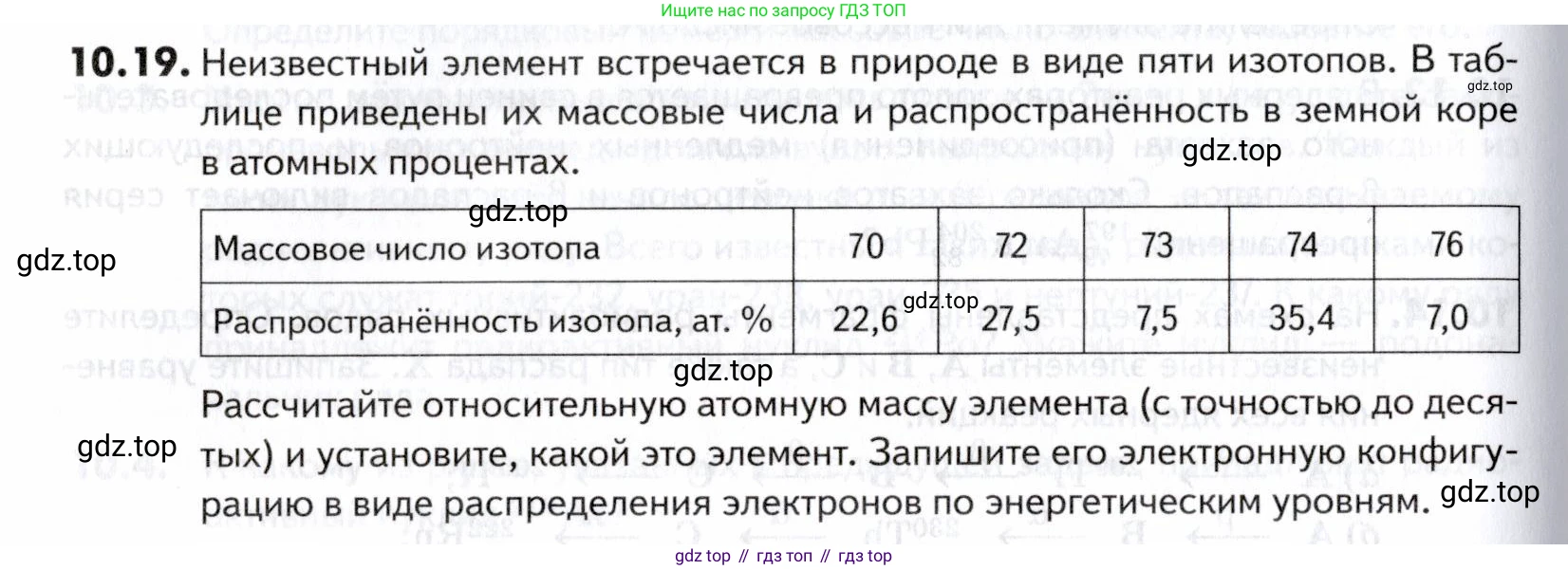
10.19. Неизвестный элемент встречается в природе в виде пяти изотопов. В таблице приведены их массовые числа и распространённость в земной коре в атомных процентах.
| Массовое число изотопа | 70 | 72 | 73 | 74 | 76 |
| Распространённость изотопаб ат. % | 22,6 | 27,5 | 7,5 | 35,4 | 7,0 |
Рассчитайте относительную атомную массу элемента (с точностью до десятых) и установите, какой это элемент. Запишите его электронную конфигурацию в виде распределения электронов по энергетическим уровням.
Решение 3. №19 (с. 252)
Дано:
Массовое число изотопа 1, $A_1 = 70$; распространённость $w_1 = 22,6\%$
Массовое число изотопа 2, $A_2 = 72$; распространённость $w_2 = 27,5\%$
Массовое число изотопа 3, $A_3 = 73$; распространённость $w_3 = 7,5\%$
Массовое число изотопа 4, $A_4 = 74$; распространённость $w_4 = 35,4\%$
Массовое число изотопа 5, $A_5 = 76$; распространённость $w_5 = 7,0\%$
Перевод процентной распространённости в дольные единицы:
$w_1 = 0,226$
$w_2 = 0,275$
$w_3 = 0,075$
$w_4 = 0,354$
$w_5 = 0,070$
Найти:
1. Относительную атомную массу элемента $A_r(Э)$ с точностью до десятитысячных.
2. Неизвестный элемент.
3. Электронную конфигурацию элемента в виде распределения электронов по энергетическим уровням.
Решение:
1. Относительная атомная масса элемента ($A_r$) — это средневзвешенное значение масс его природных изотопов с учётом их распространённости. Расчёт производится по формуле:
$A_r(Э) = \sum(A_i \cdot w_i) = A_1 \cdot w_1 + A_2 \cdot w_2 + A_3 \cdot w_3 + A_4 \cdot w_4 + A_5 \cdot w_5$
где $A_i$ — массовое число i-го изотопа, а $w_i$ — его дольная распространённость.
Подставим данные значения в формулу:
$A_r(Э) = 70 \cdot 0,226 + 72 \cdot 0,275 + 73 \cdot 0,075 + 74 \cdot 0,354 + 76 \cdot 0,070$
$A_r(Э) = 15,82 + 19,80 + 5,475 + 26,196 + 5,32 = 72,611$
Согласно условию, результат необходимо представить с точностью до десятитысячных (четыре знака после запятой), следовательно:
$A_r(Э) = 72,6110$
2. Найдём в периодической системе химических элементов Д. И. Менделеева элемент с относительной атомной массой, близкой к рассчитанному значению $72,6110$. Этому значению соответствует элемент Германий ($Ge$), порядковый номер 32, относительная атомная масса которого равна 72,63.
3. Порядковый номер элемента Германия ($Ge$) равен 32. Это означает, что заряд ядра его атома составляет +32, а общее число электронов в атоме — 32. Распределим эти электроны по энергетическим уровням:
Первый энергетический уровень (n=1): 2 электрона ($1s^2$)
Второй энергетический уровень (n=2): 8 электронов ($2s^22p^6$)
Третий энергетический уровень (n=3): 18 электронов ($3s^23p^63d^{10}$)
Четвертый (внешний) энергетический уровень (n=4): 4 электрона ($4s^24p^2$)
Таким образом, распределение электронов по энергетическим уровням записывается как последовательность чисел: 2, 8, 18, 4.
Ответ:
Относительная атомная масса элемента равна $72,6110$.
Неизвестный элемент — Германий ($Ge$).
Распределение электронов по энергетическим уровням: 2, 8, 18, 4.
Другие задания:
Помогло решение? Оставьте отзыв в комментариях ниже.
Мы подготовили для вас ответ c подробным объяснением домашего задания по химии за 10-11 класс, для упражнения номер 19 расположенного на странице 252 к задачнику 2023 года издания для учащихся школ и гимназий.
Теперь на нашем сайте ГДЗ.ТОП вы всегда легко и бесплатно найдёте условие с правильным ответом на вопрос «Как решить ДЗ» и «Как сделать» задание по химии к упражнению №19 (с. 252), авторов: Еремин (Вадим Владимирович), Дроздов (Андрей Анатольевич), Ромашов (Леонид Владимирович), ФГОС (новый, красный) учебного пособия издательства Просвещение.




















